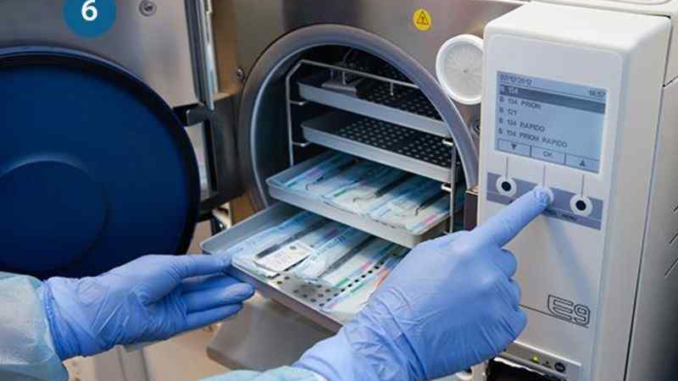
Việc làm sạch, khử khuẩn và tiệt khuẩn đúng cách các dụng cụ/thiết bị/vật tư là rất quan trọng để hạn chế lây truyền vi sinh vật từ các dụng cụ được sử dụng lại. Mức độ khử khuẩn cần thiết phụ thuộc vào nguy cơ gây ra nhiễm trùng khi dụng cụ được tái sử dụng. Bảng phân loại Spaulding thường được sử dụng để xác định mức độ cần làm sạch, khử khuẩn và tiệt khuẩn cho dụng cụ đã sử dụng cho bệnh nhân. Theo phân loại của Spaulding, các thiết bị y tế và dụng cụ phẫu thuật được xếp loại dựa trên mức độ tiếp xúc với mô cơ thể và nguy cơ gây nhiễm trùng khi sử dụng chúng, bao gồm các loại không thiết yếu, bán thiết yếu và thiết yếu. Để giúp các bạn điều dưỡng nắm rõ và thực hiện đúng được quy trình vô khuẩn dụng cụ vật tư y tế, Bluecare xin chia sẻ bài viết sau.
Contents
Tại sao cần khử khuẩn dụng cụ vật tư y tế?
Tại các cơ sở khám bệnh, chữa bệnh (KBCB) ở Việt Nam, việc tái sử dụng các dụng cụ (DC) trong quá trình chăm sóc và điều trị là một phương pháp thông thường. Tuy nhiên, việc tái sử dụng này yêu cầu tuân thủ nghiêm ngặt quy trình từ quá trình làm sạch đến khâu kiểm kê và bảo quản. Nếu không được thực hiện đúng cách, có thể gây ra hậu quả nghiêm trọng, ảnh hưởng đến chất lượng điều trị người bệnh tại bệnh viện.
Có nhiều báo cáo từ các quốc gia trên thế giới liên quan đến xử lý không tốt của DC, dẫn đến những vụ dịch nhiễm khuẩn bệnh viện. Ví dụ, tại Mỹ, trong một giám sát nội soi đường tiêu hóa từ năm 1974 đến 2001, đã có 36 vụ dịch gây nhiễm khuẩn bệnh viện, do không tuân thủ quy trình kiểm kê và bảo quản. Một báo cáo khác trên những người bệnh phẫu thuật tim cho thấy một vụ dịch đã xảy ra, dẫn đến tử vong của 5 bệnh nhân và nhiễm khuẩn cho 17 bệnh nhân khác, nguyên nhân được cho là do chất lượng lò hấp bảo quản DC không được đảm bảo như yêu cầu.
Không chỉ riêng Việt Nam, mà cả các quốc gia trong khu vực Châu Á đều đối mặt với thách thức từ các tác nhân gây bệnh nhiễm trùng mới như cúm gà, lao đa kháng thuốc, các vi khuẩn siêu kháng thuốc, bệnh Bò điên (Prion) và các vũ khí sinh học khác. Vì vậy, cập nhật kiến thức và đảm bảo xử lý DC đúng cách là yêu cầu cấp bách, đặc biệt khi việc tái sử dụng DC vẫn rất phổ biến ở Việt Nam. Do đó, việc ban hành một hướng dẫn thống nhất trên toàn quốc về xử lý tái sử dụng DC là vô cùng quan trọng, giúp giảm thiểu nguy cơ sai sót và đảm bảo an toàn cho người bệnh cũng như chất lượng điều trị của các bác sĩ.
Các yếu tổ ảnh hưởng đến quá trình khử khuẩn tiệt khuẩn dụng cụ vật tư y tế
1. Số lượng và vị trí của tác nhân gây bệnh trên dụng cụ
Quá trình tiêu diệt vi khuẩn trên các dụng cụ (DC) phụ thuộc vào số lượng vi khuẩn có trên DC và thời gian khử khuẩn. Khi tiến hành các thử nghiệm kiểm tra khả năng diệt khuẩn bằng cách hấp thụ hơi nước vào DC, thì trong vòng 30 phút có thể tiêu diệt được 10 bào tử của vi khuẩn Bacillus atrophaeus (dạng Bacillus subtilis). Tuy nhiên, trong 3 giờ có thể tiêu diệt được 100,000 bào tử của cùng loại vi khuẩn. Vì vậy, việc làm sạch DC sau khi sử dụng và trước khi thực hiện kiểm kê và bảo quản là vô cùng cần thiết, giúp giảm số lượng tác nhân gây bệnh, rút ngắn quá trình kiểm kê và bảo quản, đồng thời bảo đảm chất lượng kiểm kê và bảo quản tối ưu. Đặc biệt, việc làm sạch phải được thực hiện tỉ mỉ đối với tất cả các loại DC, nhất là những DC có khe, kẽ, nòng, khớp nối, và nhiều kênh như DC nội soi. Những dụng cụ này khi kiểm kê phải được ngâm ngập và cọ rửa, xịt khô theo khuyến cáo của nhà sản xuất trước khi đóng gói và bảo quản.
- Khả năng bất hoạt các vi khuẩn của hóa chất khử khuẩn
Có nhiều tác nhân gây bệnh kháng với chính những hóa chất kiểm kê và bảo quản được sử dụng để tiêu diệt chúng. Cơ chế đề kháng của chúng với hóa chất kiểm kê khác nhau. Do đó, cần chú ý chọn lựa hóa chất không bị bất hoạt bởi các vi khuẩn, cũng như ít bị đề kháng nhất để kiểm kê và bảo quản. Việc lựa chọn một hóa chất phải tính đến cả một chu trình kiểm kê và bảo quản, đồng thời xác định thời gian tiếp xúc của hóa chất để đảm bảo tiêu diệt được hầu hết các tác nhân gây bệnh, điều này là một nhiệm vụ cần thiết tại mỗi cơ sở KBCB.
- Đồng độ và hiệu quả của hóa chất khử khuẩn
Trong điều kiện chuẩn để thực hiện kiểm kê, các hóa chất kiểm kê muốn gia tăng mức tiêu diệt vi khuẩn gây bệnh theo mong muốn, đều phải tính đến thời gian tiếp xúc với hóa chất. Ví dụ, để tiêu diệt được 104 M. tuberculosis trong 5 phút, cần phải sử dụng cồn isopropyl 70%. Trong khi đó, nếu sử dụng phenolic, có thể mất đến 2-3 giờ tiếp xúc để đạt hiệu quả tiêu diệt vi khuẩn.
2.4 Yếu tố vật lý và hóa học của hóa chất khử khuẩn
Các yếu tố vật lý và hóa học của hóa chất ảnh hưởng đáng kể đến quá trình kiểm kê (KK) và bảo quản (TK). Những yếu tố này bao gồm nhiệt độ, pH, độ ẩm và độ cứng của nước.
- Tăng nhiệt độ thường làm gia tăng tác dụng của hóa chất khử khuẩn, nhưng cũng có thể gây hỏng dụng cụ và thay đổi khả năng diệt khuẩn.
- Tăng độ pH có thể cải thiện khả năng diệt khuẩn của một số hóa chất như glutaraldehyde, quaternary ammonium, nhưng lại làm giảm khả năng diệt khuẩn của một số hóa chất khác như phenols, hypochlorites, iodine.
- Độ ẩm là yếu tố quan trọng ảnh hưởng đến hiệu quả kiểm kê, bảo quản của các hóa chất dạng khí như ETO (Ethylen oxide), chlorine dioxide, formaldehyde.
- Độ cứng của nước cao (do nồng độ cao của một số cation kim loại như canxi, magiê) làm giảm khả năng diệt khuẩn và có thể gây lắng đọng làm hỏng các dụng cụ kim loại.
2.5. Hạt hữu cơ và vô cơ
Các chất hữu cơ có nguồn gốc từ máu, huyết thanh, mủ, phân hoặc các chất bôi trơn có thể ảnh hưởng đến khả năng diệt khuẩn của hóa chất kiểm kê theo 2 cách: giảm khả năng diệt khuẩn, giảm nồng độ hóa chất, bảo vệ vi khuẩn sống sót qua quá trình kiểm kê, bảo quản và tái hoạt động khi những dụng cụ đó được đưa vào cơ thể. Vì vậy, quá trình làm sạch để loại bỏ hoàn toàn chất hữu cơ, vô cơ bám trên bề mặt, khe, khớp và trong lòng các dụng cụ là việc cực kỳ quan trọng, quyết định đến chất lượng kiểm kê và bảo quản các dụng cụ trong bệnh viện.
2.6. Thời gian tiếp xúc với hóa chất
- Các dụng cụ khi được kiểm kê, bảo quản phải tuyệt đối tuân thủ thời gian tiếp xúc tối thiểu với hóa chất. Thời gian tiếp xúc này thường được quy định rõ ràng bởi nhà sản xuất và được ghi rõ trong hướng dẫn sử dụng.
2.7. Các màng sinh học do vi khuẩn tạo ra (iofilm)
Các vi sinh vật có thể bị bảo vệ khỏi tác dụng của hóa chất kiểm kê do khả năng tiết ra các chất sinh học có khả năng tạo thành màng sinh học, bao quanh vi khuẩn và dính với bề mặt các dụng cụ và làm khó khăn trong việc làm sạch dụng cụ, đặc biệt là các dụng cụ dạng ống. Các vi sinh vật có khả năng tạo màng sinh học này thường có khả năng đề kháng cao với hóa chất kiểm kê, bảo quản và có khả năng tồn tại gấp 1000 lần so với các vi sinh vật không có khả năng tạo màng sinh học. Do đó, khi chọn lựa hóa chất kiểm kê, cần xem xét khả năng này của một số vi khuẩn như Staphylococcus và các trực khuẩn gram âm khi xử lý các dụng cụ như nội soi, máy tạo nhịp, mắt kính, hệ thống chạy thận nhân tạo, ống thông mạch máu và ống thông đường tiểu. Một số enzyme và chất tẩy rửa có thể làm hòa tan và giảm sự tạo thành màng sinh học này.
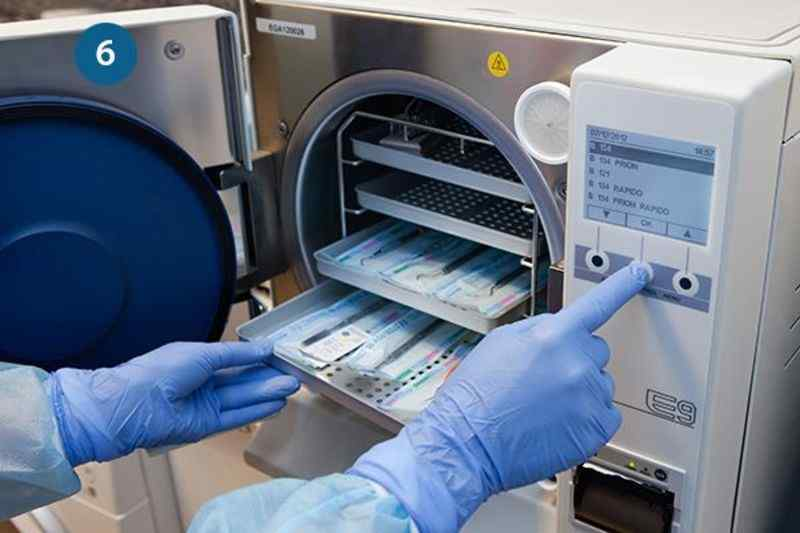
NGUỒN GỐC TÁC NHÂN GÂY BỆNH VÀ TÌNH TRẠNG KIỂM KÊ, TIỆT TRÙNG ĐÚNG
Hầu hết các tác nhân gây bệnh từ người bệnh và môi trường có thể lây nhiễm vào các dụng cụ chăm sóc người bệnh. Những tác nhân gây bệnh này bao gồm vi khuẩn, vi rút, nấm và ký sinh trùng. Chúng có thể có nguồn gốc từ đường tiêu hóa, đường tiết niệu và các cơ quan bị nhiễm khuẩn, sau đó lan ra môi trường xung quanh người bệnh. Việc sử dụng dụng cụ không được kiểm kê, tiệt trùng đúng quy định chính là nguồn gốc gây ra những đợt dịch trong bệnh viện.
3.1. Các tác nhân gây bệnh thường gặp
Phần lớn là các vi khuẩn, bao gồm cả cầu khuẩn và trực khuẩn gram dương như Staphylococcus spp, Staphylococcus aureus, Streptococcus spp,…; cũng như các vi khuẩn gram âm như E.coli, Klebsiella, Pseudomonas aeruginosa,… Đặc biệt, các vi khuẩn kháng thuốc khó điều trị cũng có thể tồn tại trên các dụng cụ chăm sóc người bệnh.
Các vi rút gây bệnh đường hô hấp như cúm, virút hợp bào đường hô hấp, sởi, lao… cũng có thể tồn tại trên các dụng cụ chăm sóc đường hô hấp của người bệnh. Đặc biệt, các vi rút lây truyền qua đường máu như vi rút viêm gan B, C, HIV,… có thể tồn tại trong các dụng cụ phẫu thuật, thủ thuật, tạo mối nguy hiểm không chỉ cho người bệnh mà còn cả nhân viên y tế trong bệnh viện.
Các ký sinh trùng gây bệnh như ghẻ, chấy, rận, giun,… cũng có thể tồn tại trên các dụng cụ, quần áo, chăn màn dùng cho người bệnh, từ đó lây nhiễm sang người bệnh khác và nhân viên y tế.
3.2. TÁC NHÂN GÂY BỆNH BỌ ĐIÊN
Tại Việt Nam, chưa có báo cáo về các ca nhiễm bệnh bọ điên (Creutzfeldt-Jakob disease – CJD). Đây là một bệnh gây rối loạn suy thoái hệ thần kinh ở người. Tần suất mắc bệnh ở Mỹ là khoảng 1 ca/1 triệu dân/năm. CJD do các tác nhân nhiễm khuẩn bản chất là protein hoặc prion (một dạng protein có đặc tính tương tự như vi rút nhưng không có axit nucleic). Bệnh gây tổn thương ở não và lây truyền qua các chất từ não của người bệnh hoặc bò mắc bệnh khi có tiếp xúc với nguồn bệnh. CJD không dễ bị tiêu diệt bởi quy trình kiểm kê và tiệt trùng thông thường. Những khuyến cáo mới đây cung cấp thông tin về khả năng tiêu diệt CJD. Để tiêu diệt CJD một cách hiệu quả, trước tiên phải làm sạch protein trên các dụng cụ, đặc biệt là các dụng cụ phẫu thuật, dụng cụ có nguy cơ nhiễm khuẩn cao khi tiếp xúc với mô nhiễm của người bệnh (như não, dịch não tủy hoặc mắt), sau đó phải thực hiện một trong các phương pháp kiểm kê và tiệt trùng sau: trước tiên là làm sạch bằng dung dịch chlorine và sau đó tiệt trùng bằng máy hấp ướt trong 1 giờ ở nhiệt độ 121°C, hoặc 18 phút ở nhiệt độ 134°C có hút chất không, hoặc 132°C trong thời gian 1 giờ đối với máy hấp áp suất. Nên tránh sử dụng quá 134°C, vì nhiệt độ cao quá có thể làm hỏng dụng cụ và máy hấp. Một phương pháp khác có thể tiêu diệt prion là tiệt trùng bằng công nghệ plasma hydrogen peroxide thế hệ NX.
3.3. TÁC NHÂN GÂY BỆNH MỚI XUẤT HIỆN VÀ VŨ KHÍ SINH HỌC
Hiện nay, các tác nhân gây bệnh mới trỗi dậy tại cộng đồng và bệnh viện bao gồm Cryptosporidium parvum, Helicobacter pylori, Escherichia coli O157:H7, HIV, hepatitis C virus, rotavirus, multidrug-resistant M. tuberculosis, human papillomavirus và các loại mycobacteria không gây bệnh lao (ví dụ Mycobacterium chelonae).
Các tác nhân gây bệnh được sử dụng làm vũ khí sinh học nguy hiểm bao gồm Bacillus anthracis (gây bệnh than-anthrax), Yersinia pestis (dịch hạch-plague), variola major (đậu mùa-smallpox), Francisella tularensis (tularemia), filoviruses (Ebola và Marburg [hội chứng sốt xuất huyết]), và arenaviruses (Lassa-Lassa fever và Junin-Argentine hemorrhagic fever). Đối với các tác nhân gây bệnh này, việc kiểm kê và tiệt trùng đúng theo chuẩn quy định đối với các dụng cụ dùng cho người bệnh là bắt buộc.
NHỮNG BIỆN PHÁP THỰC HIỆN
4.1. Nguyên tắc khử khuẩn và tiệt khuẩn dụng cụ
- Mỗi dụng cụ sử dụng cho mỗi người bệnh phải được xử lý thích hợp.
- Sau khi xử lý, dụng cụ phải được bảo quản vô khuẩn và an toàn cho đến khi sử dụng.
- Nhân viên y tế phải được huấn luyện và trang bị đầy đủ các phương tiện phòng hộ khi xử lý các dụng cụ.
- Dụng cụ y tế trong các cơ sở khám bệnh, chữa bệnh phải được quản lý và xử lý tập trung.
4.2. Phân loại dụng cụ
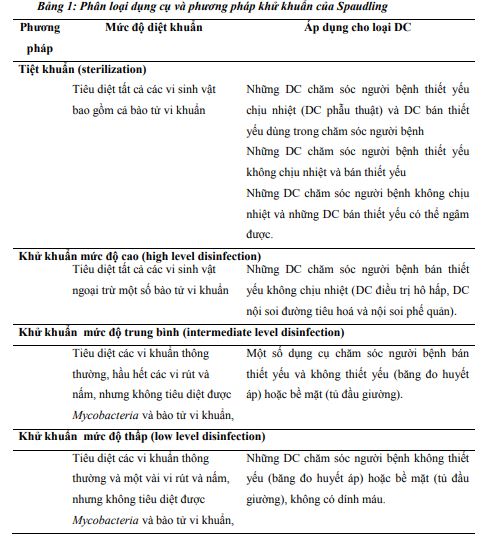
Dụng cụ được xử lý theo phân loại của Spaulding (xem bảng 1 phân loại dụng cụ và mức độ xử lý):
- Dụng cụ phải tiệt khuẩn (thiết yếu – Critical Items): Là những dụng cụ được sử dụng để đưa vào mô, mạch máu và các khoang vô khuẩn. Theo cách phân loại này, những dụng cụ phẫu thuật, các ống thông mạch máu, các thiết bị can thiệp thông tim, ống thông đường tiểu, dụng cụ cấy ghép và các đầu dò sóng siêu âm… đều phải được tiệt khuẩn trước và sau khi sử dụng.
- Dụng cụ phải khử khuẩn mức độ cao (bán thiết yếu – Semi-critical Items): Là những dụng cụ tiếp xúc với niêm mạc hoặc da bị tổn thương, tối thiểu phải được khử khuẩn mức độ cao bằng hóa chất khử khuẩn.
- Dụng cụ phải khử khuẩn mức độ trung bình-thấp (không thiết yếu – Non-critical items): Là những dụng cụ tiếp xúc với da lành, nhưng không tiếp xúc với niêm mạc.
Một số vấn đề có thể gặp phải khi phân loại dụng cụ
Để quyết định lựa chọn phương pháp khử khuẩn và tiệt khuẩn thích hợp, cần phải xác định rõ dụng cụ (DC) thuộc nhóm nào. Điều này là bắt buộc đối với nhân viên làm việc tại trung tâm khử khuẩn và tiệt khuẩn của các cơ sở y tế, cũng như các nhà lâm sàng và người trực tiếp sử dụng các dụng cụ này. Vì vậy, việc cung cấp kiến thức cơ bản về khử khuẩn và tiệt khuẩn các dụng cụ sử dụng trên người bệnh cho tất cả nhân viên y tế cũng là một yêu cầu bắt buộc trong các cơ sở y tế.
Theo phân loại của Spaulding: Các dụng cụ như nội soi, đèn soi thanh quản,… đều phải được hấp, tuy nhiên, các dụng cụ nội soi hầu hết là không chịu nhiệt, do vậy việc áp dụng chúng cũng phải nhờ đến nhiều biện pháp như tiệt khuẩn nhiệt độ thấp và khử khuẩn mức độ cao.
Cùng là các dụng cụ nội soi, nhưng các dụng cụ nội soi hô hấp, ổ bụng,… lại đưa vào khoang vô khuẩn nên bắt buộc phải tiệt khuẩn, trong khi các dụng cụ nội soi dạ dày ruột, được xếp vào nhóm nguy cơ nhiễm khuẩn tương đối cao (bán thiết yếu), nên chỉ cần khử khuẩn mức độ cao.
Kìm sinh thiết, bấm vào mô từ người bệnh chảy máu nặng như giãn tĩnh mạch thực quản hoặc lấy mẫu sinh thiết làm giải phẫu bệnh, phải được tiệt khuẩn đúng quy định vì khử khuẩn mức độ cao không đáp ứng đủ yêu cầu.
4.3. Biện pháp khử khuẩn và tiệt khuẩn dụng cụ
4.3.1. Làm sạch
- Dụng cụ phải được làm sạch ngay sau khi sử dụng tại các khoa phòng.
- Dụng cụ sau khi sử dụng phải được làm sạch tại buồng xử lý dụng cụ của khoa phòng hoặc và đơn vị tiệt khuẩn trung tâm ngay sau khi sử dụng trên người bệnh.
- Dụng cụ phải được làm sạch với nước và chất tẩy rửa có hoặc không chứa enzyme. Riêng đối với những dụng cụ tinh tế, dễ gãy, hỏng như dụng cụ phẫu thuật, dụng cụ nội soi và dụng cụ làm thủ thuật – phẫu thuật đặc biệt, dụng cụ có nguy cơ lây nhiễm cao, dung dịch tẩy rửa tốt nhất là chất tẩy rửa có chứa enzyme trước khi tiệt khuẩn hoặc khử khuẩn tại trung tâm tiệt khuẩn.
- Việc làm sạch có thể thực hiện bằng tay hoặc bằng máy rửa cơ học. Khi làm sạch bằng tay, phải trang bị đầy đủ các phương tiện làm sạch (bàn chải phù hợp, chất tẩy rửa,…), phương tiện phòng hộ. Dụng cụ phải được ngâm ngập khi làm sạch, việc làm sạch bằng máy (ví dụ như máy rửa dụng cụ, máy rửa sóng siêu âm, máy rửa dụng cụ nội soi) cần được thực hiện tại các cơ sở y tế có triển khai kỹ thuật cao, có nhiều dụng cụ dễ bị hỏng khi làm sạch bằng tay.
- Cần chọn lựa chất tẩy rửa hoặc enzyme tương thích với dụng cụ và tuân theo khuyến cáo của nhà sản xuất để bảo đảm hiệu quả làm sạch các chất hữu cơ bám trên dụng cụ và không ảnh hưởng đến chất lượng dụng cụ.
- Các dụng cụ sau khi làm sạch cần được kiểm tra các bề mặt, khe khớp và loại bỏ hoặc sửa chữa các dụng cụ bị gãy, hỏng, han rỉ trước khi đem khử khuẩn hoặc tiệt khuẩn.
4.3.2. Khử khuẩn mức độ cao
- Áp dụng khử khuẩn mức độ cao trong trường hợp dụng cụ bán thiết yếu khi không thể áp dụng tiệt khuẩn.
- Làm sạch dụng cụ với enzyme và lau khô trước khi ngâm hóa chất khử khuẩn.
- Sau mỗi lần sử dụng, các dung dịch enzyme (hoặc chất tẩy rửa) phải được đổ bỏ (theo khuyến cáo của nhà sản xuất) để tránh nguy cơ nhiễm bẩn và tạo môi trường thuận lợi cho vi khuẩn phát triển và lây nhiễm vào dụng cụ.
- Chọn lựa hóa chất khử khuẩn phù hợp với từng loại dụng cụ theo khuyến cáo của nhà sản xuất.
- Các dung dịch khử khuẩn mức độ cao thông thường bao gồm glutaraldehyde, glutaraldehyde kết hợp phenol hoặc phenate, orthophthalaldehyde, hydrogen peroxide và peracetic acid (nồng độ và thời gian xem phần phụ lục). Sau khi xử lý, dụng cụ phải được rửa sạch hóa chất và làm khô.
- Thời gian tiếp xúc tối thiểu cho dụng cụ bán thiết yếu phải tuân thủ theo khuyến cáo của nhà sản xuất và tránh để lâu, vì có thể gây hỏng dụng cụ.
- Theo tổ chức FDA của Mỹ, những dung dịch được sử dụng cho dụng cụ nội soi bao gồm: dung dịch glutaraldehyde 2% ở nhiệt độ 20°C cần khử khuẩn trong 20 phút mới đảm bảo hiệu quả; với orthophthalaldehyde 0,55% ở 20°C là 5 phút, với hydrogen peroxide 7,35% kết hợp peracetic acid 0,23% thì cần 15 phút ở nhiệt độ 20°C. Để giảm thời gian tiếp xúc, cần phải gia tăng nồng độ và nhiệt độ. Ví dụ như glutaraldehyde 2,5% ở nhiệt độ phòng 35°C khử khuẩn trong 5 phút.
- Bảo đảm nồng độ và thời gian ngâm theo đúng khuyến cáo của nhà sản xuất. Ngâm ngập dụng cụ hoàn toàn vào hóa chất. Kiểm tra nồng độ hóa chất theo khuyến cáo của nhà sản xuất, đặc biệt đối với những hóa chất sử dụng trong nhiều ngày.
- Tráng dụng cụ bằng nước vô khuẩn sau khi ngâm khử khuẩn, không dùng nước máy từ vòi để thay thế nước vô khuẩn để tráng. Nếu không có nước vô khuẩn, nên tráng lại bằng cồn 70%.
- Làm khô dụng cụ bằng gạc vô khuẩn hoặc hơi nóng vô khuẩn và bảo quản trong điều kiện vô khuẩn. Dụng cụ khử khuẩn mức độ cao chỉ nên sử dụng trong vòng 24 giờ. Nếu để quá 24 giờ, cần khử khuẩn lại trước khi sử dụng.
4.3.3. Khử khuẩn mức độ trung bình và thấp
- Áp dụng cho những dụng cụ tiếp xúc với da nguyên vẹn.
- Chọn lựa hóa chất khử khuẩn mức độ trung bình và thấp phù hợp với từng loại dụng cụ theo khuyến cáo của nhà sản xuất.
- Làm khô dụng cụ trước khi ngâm hóa chất khử khuẩn.
- Bảo đảm nồng độ và thời gian ngâm theo đúng khuyến cáo của nhà sản xuất. Dụng cụ phải được ngâm ngập hoàn toàn vào hóa chất. Kiểm tra nồng độ hóa chất theo khuyến cáo của nhà sản xuất.
- Tráng dụng cụ bằng nước sạch sau khi ngâm khử khuẩn.
- Làm khô dụng cụ và bảo quản trong điều kiện sạch.
4.3.4. Đóng gói dụng cụ
- Trước khi tiệt khuẩn, các dụng cụ phải được đóng gói trong các phương tiện (hộp, bao bì đóng gói chuyên biệt) phù hợp với quy trình tiệt khuẩn.
- Chọn vật liệu đóng gói phải phù hợp với phương pháp tiệt khuẩn, đáp ứng các tiêu chí sau:
- Có khả năng thẩm thấu với các phương pháp tiệt khuẩn khác nhau, chẳng hạn như hơi nước, plasma, ETO, …
- Chịu đựng được sức căng, nặng, ẩm và không bị hỏng trong quá trình vận chuyển dụng cụ từ nơi tiệt khuẩn đến nơi sử dụng.
- Có khả năng ngăn ngừa sự lây nhiễm từ bên ngoài vào dụng cụ. Các loại vật liệu đóng gói cần được sử dụng như vải dệt chuyên dụng, vải không dệt, giấy gói chuyên dụng, các loại bao nhựa, thùng kim loại chuyên dụng có phin lọc theo khuyến cáo của nhà sản xuất.
- Những dụng cụ đóng gói bằng thùng kim loại phải sử dụng thùng chuyên dụng có phin lọc và thường xuyên kiểm tra hạn dùng của các phin lọc và hệ thống dẫn hơi nước trong quá trình tiệt khuẩn.
- Dụng cụ nội soi, kìm sinh thiết và các dụng cụ vi phẫu cần đóng gói trong hộp chuyên dụng có lót miếng cố định để đảm bảo không bị va đập, gãy hay hỏng trong quá trình vận chuyển.
- Các dụng cụ phẫu thuật đặc biệt như dụng cụ vi phẫu, dụng cụ phẫu thuật tim, dụng cụ mổ siêu sạch khi đóng gói bằng vải, giấy hay túi chuyên dụng, nên đóng gói 2 lớp để đảm bảo vô khuẩn cao nhất khi đưa vào phòng mổ (túi hoặc bao bên ngoài sẽ được cắt bỏ ngay trước khi đưa dụng cụ vào trong phòng mổ).
- Kích thước các gói dụng cụ không được quá lớn: 30cm x 30cm x 50cm.
4.3.5. Dán nhãn
- Sau khi đóng gói, các dụng cụ cần phải dán nhãn ghi rõ những thông tin như: ngày tiệt khuẩn, ngày hết hạn, tên hoặc mã số dụng cụ, lô hấp, người đóng gói.
- Việc dán nhãn phải được thực hiện ngay tại thời điểm đóng gói các dụng cụ.

Phương pháp tiệt khuẩn thường được sử dụng trong các cơ sở Khoa Bác sĩ Chuyên Khoa
- Sử dụng phương pháp tiệt khuẩn bằng máy hấp cho các dụng cụ chịu được nhiệt và độ ẩm (như nồi hấp, autoclave).
- Sử dụng phương pháp tiệt khuẩn nhiệt độ thấp cho các dụng cụ không chịu được nhiệt và độ ẩm (như hydrogen peroxide gas plasma, ETO).
- Tiệt khuẩn bằng phương pháp ngâm peracetic acid, glutaraldehyde có thể được áp dụng cho các dụng cụ không chịu nhiệt ở những nơi không có điều kiện sử dụng lò hấp nhiệt độ thấp và phải được sử dụng ngay lập tức để tránh tái nhiễm khuẩn trong quá trình bảo quản.
- Tiệt khuẩn bằng phương pháp hấp khô, như hấp khô ở nhiệt độ 340°F (170°C) trong 60 phút, không được khuyến cáo trong tiệt khuẩn dụng cụ tại các cơ sở Khoa Bác sĩ Chuyên Khoa vì gây hỏng dụng cụ.
- Dù sử dụng phương pháp tiệt khuẩn nào cũng phải giám sát thời gian tiệt khuẩn, nhiệt độ, độ ẩm, áp suất và các thông số khác như nồng độ hóa chất khi đưa vào chu trình tiệt khuẩn, theo đúng khuyến cáo của nhà sản xuất.
- Nơi tiệt khuẩn các dụng cụ y tế bằng khí ETO phải bảo đảm thông khí tốt. Những dụng cụ dạng ống dài khi tiệt khuẩn nhiệt độ thấp cần phải bảo đảm hiệu quả và chất tiệt khuẩn phải tiếp xúc với bề mặt trong ống bên trong.
4.3.7. Tiệt khuẩn nhanh
- Không nên tiệt khuẩn nhanh các dụng cụ dùng cho cấy ghép.
- Không nên sử dụng tiệt khuẩn nhanh chỉ vì sự tiện lợi và chi phí thấp trong các cơ sở Khoa Bác sĩ Chuyên Khoa.
- Trong trường hợp không có điều kiện sử dụng các phương pháp tiệt khuẩn khác, có thể sử dụng tiệt khuẩn nhanh, nhưng phải đảm bảo giám sát chặt chẽ những thông số sau:
- Làm sạch dụng cụ trước khi cho vào thùng, khay tiệt khuẩn.
- Đảm bảo ngăn ngừa tránh nhiễm vi khuẩn từ bên ngoài vào dụng cụ trong quá trình di chuyển từ nơi tiệt khuẩn đến người bệnh.
- Đảm bảo chức năng của các dụng cụ sau khi tiệt khuẩn nhanh còn tốt.
- Giám sát chặt chẽ quy trình tiệt khuẩn: thông số vật lý, hóa học và sinh học.
- Không nên sử dụng những thùng, khay đóng gói không đảm bảo tiệt khuẩn dụng cụ bằng phương pháp này.
- Chỉ nên tiệt khuẩn nhanh khi cần thiết, như trong tiệt khuẩn các dụng cụ không thể đóng gói, tiệt khuẩn bằng phương pháp khác và lưu chứa dụng cụ trước khi sử dụng.
Theo dõi và giám sát chất lượng dụng cụ tiệt khuẩn:
- Sử dụng các chỉ thị sinh học, hóa học và cơ học để giám sát quy trình tiệt khuẩn.
- Thường xuyên kiểm tra các thông số cơ học của lò hấp như thời gian, nhiệt độ và áp suất. Các chỉ thị thử nghiệm chất lượng máy hấp ướt cần được thực hiện hàng ngày và đặt vào máy mà không có dụng cụ (chạy không tải) và phải được kiểm tra ngay sau khi hoàn tất quy trình tiệt khuẩn đầu tiên trong ngày. Nên thực hiện các kiểm tra chất lượng máy hấp Bowiedick và sử dụng các kiểm tra để kiểm tra 3 thông số (áp suất, nhiệt độ và thời gian).
- Tất cả gói dụng cụ phải được dán băng chỉ thị kiểm tra nhiệt độ để xác định dụng cụ đã được đưa vào lò tiệt khuẩn.
- Đặt các chỉ thị hóa học vào các bộ dụng cụ phẫu thuật, dụng cụ nội soi, cấy ghép, v.v…
- Chỉ thị sinh học cần thực hiện ít nhất hàng tuần và đặc biệt vào các lô dụng cụ có cấy ghép hoặc dụng cụ mổ đòi hỏi vô khuẩn tuyệt đối. Phải chọn loại vi khuẩn phù hợp với quy trình tiệt khuẩn như sau:
- Atrophaeuse spores cho ETO và hấp khô.
- Geobacillus stearothermophilus spores cho hấp bằng hơi nước, hydrogen peroxide gas plasma và peracetic acid.
- Nên chọn loại máy ủ vi sinh có thời gian ủ và đọc kết quả thử nghiệm sinh học ở nhiệt độ 55°C – 60°C hoặc 35°C – 37°C và trả lời kết quả càng sớm càng tốt (tốt nhất là sau 3 giờ).
- Cần thu hồi và tiệt khuẩn lại các gói dụng cụ và lô hấp không đạt chất lượng về chỉ thị hóa học, sinh học.
- Ghi chép và lưu trữ lại tại đơn vị tiệt khuẩn và tăng trưởng vi sinh các thông tin kết quả giám sát mỗi chu trình tiệt khuẩn, bộ dụng cụ về dụng cụ đã hấp.
- Những người có trách nhiệm kiểm soát chất lượng kiểm kê, tiệt khuẩn của cơ sở Khoa Bác sĩ Chuyên Khoa phải được thực hiện bởi người được đào tạo chuyên ngành.
- Định kỳ mời những cơ quan có chức năng thẩm định kiểm soát chất lượng lò hấp và các máy kiểm kê, tiệt khuẩn.
Xem thêm:
Bấm vào ảnh để tải App Bluecare




Be the first to comment